Zur Energiewende gehört es, die zeitweise auftretenden Überschüsse an Strom aus erneuerbaren Quellen sinnvoll zu verwenden. Eine Möglichkeit ist dabei die elektrolytische Erzeugung von Wasserstoff. Dieser grüne Wasserstoff kann dann entweder selbst als Energieträger dienen oder für weitere Synthesen genutzt werden. Denkbar ist etwa die Reaktion mit Kohlendioxid zu Methan, was zugleich helfen würde, CO2-Emissionen zu reduzieren. Das Methan wiederum ließe sich dann als Erdgasersatz verwenden. Doch auf diesem Weg gibt es einige technische Herausforderungen. So wird bei der Reaktion viel Wärme frei, die Probleme bereiten kann. Eine Forschungsgruppe des Max-Planck-Instituts für Dynamik komplexer technischer Systeme stellt nun ein neuartiges Katalysatorkonzept vor, das eine zu starke Erhitzung eines Reaktors verhindert.

Der weitere Ausbau erneuerbarer Energien wird zunehmend für Phasen sorgen, in denen mehr Strom erzeugt als akut nachgefragt wird. Da ist es wichtig, diese Überschüsse speichern zu können. Dafür eignen sich zum Beispiel Batterieanlagen. Möglich ist aber auch, den Energie-Überschuss für die Synthese chemischer Substanzen zu verwenden, die dann selbst als Energieträger oder auch als Rohstoff dienen. Ein Konzept, das auch als Power-to-X-Konzept bekannt ist. Mögliche Substanzen sind etwa Wasserstoff, Methanol und Ammoniak.
Auch Methan wäre ein sinnvoller Speicher für grüne Energie. Es könnte zum Beispiel fossiles Erdgas ersetzen, dessen Hauptbestandteil es schließlich ist. Methan lässt sich über die sogenannte Methanisierung von Kohlendioxid (CO2) gewinnen, bei der Wasserstoff und CO2 miteinander reagieren. Den Wasserstoff dafür würde man gewinnen, indem besagte Stromüberschüsse für die Elektrolyse von Wasser genutzt werden. Das Kohlendioxid wiederum könnte aus industriellen Abgasen, zum Beispiel von Zement-, Stahl- oder Kraftwerken sowie aus Biogasanlagen stammen. Das würde zugleich CO2-Emissionen verhindern und den Kohlenstoff im industriellen Stoffkreislauf halten.
Katalysator mit aktivem Kern und inaktiver Schale
Großtechnische Anlagen für die Methanisierung, die erneuerbare Energie speichern, gibt es bislang allerdings nicht. Das liegt auch an prozesstechnischen Herausforderungen. So setzt die Reaktion von CO2 und Wasserstoff viel Wärme frei, was die Temperatur in den Reaktoren stark steigen lässt. Sie darf aber nicht über 550 Grad Celsius klettern, weil sonst das als Katalysator verwendete Nickel inaktiviert würde, womit die Reaktion zum Erliegen käme.
Es sind also Konzepte gefragt, bei denen die Erwärmung Reaktor begrenzt wird. Zwar gibt es eine ganze Reihe technischer Ansätze, doch viele davon sind aufgrund eines hohen Aufwands unwirtschaftlich. Über den Pilotanlagen-Maßstab hinaus hat es bisher kein Verfahren geschafft. Forscher des Max-Planck-Instituts für die Dynamik komplexer technischer Systeme in Magdeburg haben nun ein Konzept entwickelt, das ökonomisch interessante Methan-Ausbeuten liefert und den Temperaturanstieg trotzdem im Rahmen hält. Dabei hat das Team um Kai Sundmacher, Direktor der Abteilung Prozesstechnik am Magdeburger Max-Planck-Institut für Dynamik komplexer technischer Systeme die Idee sogenannter Kern-Schale-Katalysatorpellets weiterentwickelt. „Mit diesem Aufbau aus einem katalytisch aktiven Kern und einer inaktiven Schale ist es möglich, die Reaktortemperatur zu begrenzen und so die Grundlage für eine großtechnische Methanisierung von Kohlendioxid zu schaffen“, erklärt Kai Sundmacher.
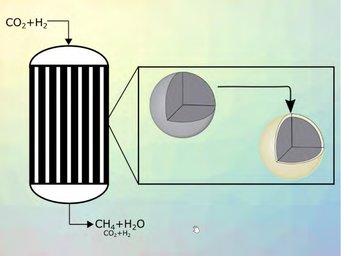
Der Clou an dem Kern-Schale-Ansatz ist die chemisch inerte poröse Schale. Moleküle, die miteinander reagieren sollen, müssen zunächst diese Hülle durchdringen, um an die Nickel-Oberfläche zu gelangen, mit der der Kern beschichtet ist. Erst dort bildet sich das Methan. „Diese Diffusion der Reaktionspartner durch die Schale ist gerade das, was die Umsetzungsrate und damit auch einen möglicherweise zu starken Temperaturanstieg bremst“, erklärt Ronny Tobias Zimmermann, Chemieingenieur im Team von Sundmacher. Mehr noch: Man habe sogar in der Hand, durch die Schalen-Eigenschaften wie etwa den Durchmesser oder die Porosität festzulegen, wie heiß der Reaktor maximal werden kann. „Je dicker die Schale, desto geringer die maximal mögliche Temperatur“, erklärt Zimmermann den Zusammenhang. Einfach weil dann der längere Weg der einzelnen Moleküle zum Katalysator die Reaktion stärker bremst.
Ein Konzept für ein schwankendes Wasserstoffangebot
Die optimalen Eigenschaften und Maße des Kern-Schale-Katalysators und auch des Reaktors ermittelte das Magdeburger Team über Computersimulationen und anschließende Experimente. Es kristallisierte sich ein Ansatz heraus, bei dem man ein Bündel aus drei Meter langen, wenige Zentimeter dicken Röhren als Reaktor verwendet, die dann jeweils mit den Kern-Schale-Katalysatorpellets gefüllt werden. Diese sind etwa drei Millimeter groß, wobei die Schale gerade einmal 0,1 Millimeter dünn ist, was etwa der doppelten Dicke eines menschlichen Haares entspricht. Für die Methanisierung leitet man ein Gemisch aus Wasserstoff und Kohlendioxid durch die auf etwa 300 Grad Celsius temperierten Röhren. Das entstehende Methangas wird am anderen Ende der Röhren aufgefangen, gereinigt und kann dann zum Beispiel in Tanks oder ins bestehende Erdgasnetz eingespeist werden.
„Alles ist so konzipiert, dass der Reaktor nie heißer als etwa 480 Grad Celsius wird, egal wie viel Ausgangsmaterial wir zuführen“, erklärt Zimmermann.
Zu einer Inaktivierung des Nickels kann es also nicht kommen. Diese Flexibilität und Robustheit ist gerade im Hinblick auf den Einsatz erneuerbarer Energien wichtig, die mal mehr, mal weniger Überschussstrom liefern. Dem wechselnden Stromangebot entsprechend schwankt auch die Menge an Wasserstoff, die erzeugt wird und mit Kohlendioxid reagieren kann. Für die Prozesstechnik sind solche Schwankungen in der Menge der Reaktionspartner generell eine große Herausforderung. Lösungen, die mit den Schwankungen gut zurechtkommen, heißen auch lastflexibel.
Vielfältige Anwendungen für Kern-Schale-Katalysatoren
„Man kann das Problem natürlich umgehen, indem man den Wasserstoff zwischenspeichert und dann konstant abruft“, sagt Kai Sundmacher. „Allerdings sind solche Speicher sehr kostenintensiv.“
Daher sei eine lastflexible Lösung wie die jetzt entwickelte von großem Interesse. Mögliche Einsatzorte ihres Reaktors für die Methangewinnung sieht das Magdeburger Team prinzipiell überall dort, wo Überschüsse an erneuerbarem Strom für den nötigen Wasserstoff sorgen können. Bei Windparks ebenso wie bei größeren Fotovoltaikanlagen.
Die Max-Planck-Forscher merken an, dass ihr Ansatz nicht nur für die Reaktion von Wasserstoff mit Kohlendioxid in Frage kommt. Generell sei das Konzept der maßgeschneiderten Kern-Schale-Katalysatoren vielmehr auf alle Gasreaktionen mit starker Wärmeentwicklung übertragbar. So auch für die Umsetzung von Wasserstoff mit Stickstoff zu Ammoniak. Aktuell ist das Magdeburger Institut auch an einem Strang des H2Mare-Projekts beteiligt. Darin geht es generell um die direkte Nutzung des Überschussstroms von Offshore-Windanlagen zur Wasserstofferzeugung. Bei der möglichen Weiterverwendung des gewonnenen Wasserstoffs werden auch die Reaktoren mit Kern-Schale-Katalysatoren zur Bildung von Methan oder Ammoniak untersucht.
Kai Sundmacher und sein Team sehen jedenfalls noch ein riesiges Potenzial für die Speicherung erneuerbaren Stroms in Chemikalien und Energieträgern. Limitierend sei derzeit vor allem die Menge an erneuerbarer Energie. Etwas, das sich aber in Zukunft ändern dürfte.
Originalveröffentlichungen
Ronny Tobias Zimmermann, Sebastian Weber, Jens Bremer, Vesselin Idakiev, Reihaneh Pashminehazar , Thomas Lennon Sheppard, Lothar Mörl, Kai Sundmacher; “Core–shell catalyst pellets for effective reaction heat management“; Chemical Engineering Journal, 1. Februar 2023; https://doi.org/10.1016/j.cej.2022.140921
Ronny Tobias Zimmermann, Jens Bremer und Kai Sundmacher; “Load-flexible fixed-bed reactors by multi-period design optimization“; Chemical Engineering Journal, 15. Januar 2022; https://doi.org/10.1016/j.cej.2021.130771
Kontakte

Prof. Dr.-Ing. Kai Sundmacher
Tel.: +49 391 6110-350 +49 391 6110-353
E-Mail: sundmacher@mpi-magdeburg.mpg.de
Dr. Ronny Tobias Zimmermann
Tel.: +49 391 6110-360
E-Mail: zimmermannr@mpi-magdeburg.mpg.de
Source
Max-Planck-Institut für Dynamik komplexer technischer Systeme, Pressemitteilung, 2023-11-29.
Supplier
Max-Planck-Institut für Dynamik komplexer technischer Systeme
Share
Renewable Carbon News – Daily Newsletter
Subscribe to our daily email newsletter – the world's leading newsletter on renewable materials and chemicals















