 Die Erforschung der Hanfpflanze Cannabis sativa hat in den letzten Jahren durch die zunehmende Legalisierung einen enormen Aufschwung erfahren. Nach einer jahrzehntelangen Verbotsphase beginnen Forscher, Ärzte und Gesetzgeber, die Scheu vor einer der ältesten Nutzpflanzen abzulegen.1 Cannabis wird schon seit Jahrtausenden als Genussmittel und Medizin konsumiert.
Die Erforschung der Hanfpflanze Cannabis sativa hat in den letzten Jahren durch die zunehmende Legalisierung einen enormen Aufschwung erfahren. Nach einer jahrzehntelangen Verbotsphase beginnen Forscher, Ärzte und Gesetzgeber, die Scheu vor einer der ältesten Nutzpflanzen abzulegen.1 Cannabis wird schon seit Jahrtausenden als Genussmittel und Medizin konsumiert.
Die Potentiale von Cannabisberuhen auf der Fähigkeit der chemischen Bestandteile, das Endocannabinoid-System (ECS) zu aktivieren und zu beeinflussen, ein homöostatisches Regulationssystem, das in allen Wirbeltieren vorhanden ist.1 Heutzutage wird Cannabis in einer Vielzahl von Ländern weltweit verwendet, aber aufgrund des eingeschränkten Zugangs zur Forschung ist unser Verständnis seines therapeutischen Potenzials und seiner Grenzen lückenhaft. In den letzten Jahrzehnten wurden mehr Untersuchungen zum Verständnis des ECS und der Rolle von Cannabis als therapeutisches Mittel durchgeführt. Obwohl Cannabis für zahlreiche therapeutische Szenarien von Vorteil ist, gibt es Hinweise darauf, dass die Wirksamkeit nicht bei allen Erkrankungen gleich hoch ist.
Cannabis ist ein evolutionäres Nebenprodukt einer Pflanze, das sich entwickelt hat, um das ECS zu beeinflussen. Das ECS ist ein biologisches System aus Rezeptoren, Liganden und Enzymen, das auf aquatische Arten 400 Millionen Jahre vor der Ankunft von Pflanzen und Bäumen zurückgeht.2 Auch der menschliche Körper produziert ständig endogene Cannabinoide – Endocannabinoide. Somit brachte uns Cannabis im Labor zum ECS, aber in der Natur führte das ECS zu Cannabis.
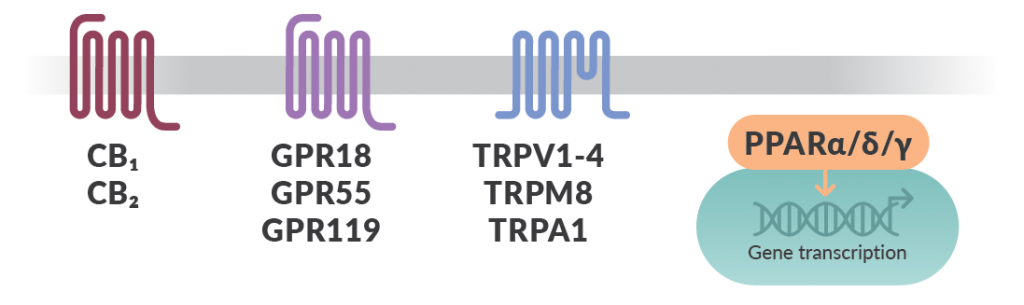
Chemisch gesehen ist Cannabis ein Gemisch aus über 500 Verbindungen.3 Am bemerkenswertesten sind Substanzen aus drei Kategorien: Phytocannabinoide (wie Δ9-THC und CBD), Terpenoide und Flavonoide.3 Phytocannabinoide wie Δ9-THC und CBD beeinflussen den Körper durch ihre Aktivitäten an G-Protein-gekoppelten Rezeptoren wie dem Cannabinoid-Rezeptor 1 (CB1) und dem Cannabinoid-Rezeptor 2 (CB2) sowie dem GPR55. Obwohl es immer mehr Hinweise auf verwandte Rezeptoren gibt, die von Cannabinoiden beeinflusst werden, wie z.B. die Transient-Receptor-Potential (TRP)-Kanäle und die Peroxisom-Proliferator-aktivierten Rezeptoren (PPARs), blieb dies bisher von der Öffentlichkeit weitgehend unbemerkt (Abbildung 1).1 Sowohl TRP- als auch PPAR-Rezeptoren spielen eine wichtige Rolle in vielen bioregulatorischen Abläufen.
Zum Beispiel ist TRPV1 für seine Rolle bei der Regulation der Körpertemperatur sowie der Empfindung von Hitze und Schmerz bekannt und PPARγ, welches in fast allen Geweben exprimiert wird, ist essentiell für Signalwege, die an der zellulären Differenzierung und Entwicklung beteiligt sind.
In vivo und in vitro wurde nachgewiesen, dass isolierte Cannabinoide und Cannabisextrakte in der Lage sind, die Apoptose in Krebszellen zu induzieren und als therapeutisches Mittel bei anderen chronischen Krankheiten zu wirken.4 Deshalb wurden bereits mehrere Arzneimittel mit Cannabinoiden oder synthetischen Cannabinoid-Verbindungen auf den Markt gebracht. Zuletzt wurde Epidiolex® von der FDA als erstes aus Cannabis gewonnenes Arzneimittel mit nur einem einzigen aktiven Wirkstoff (CBD) zugelassen. Obwohl immer mehr Staaten beginnen medizinisches Marihuana zu verwenden, ist unser Verständnis von der Wirkung von Cannabis noch unvollständig.
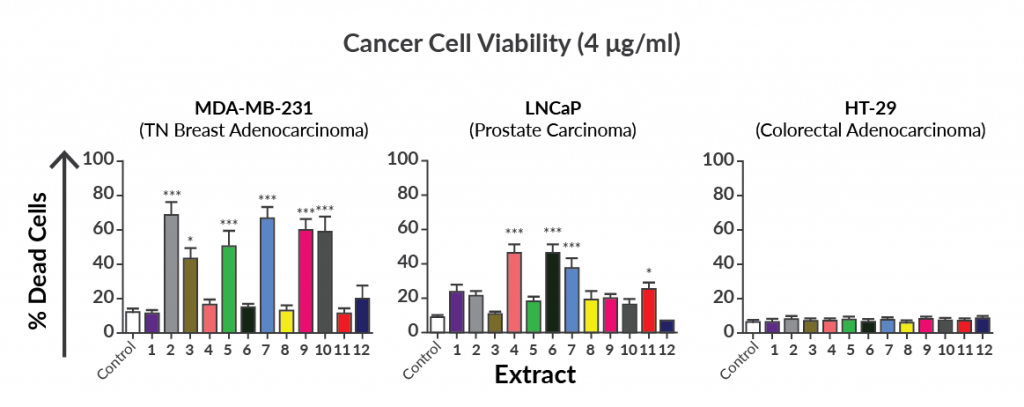
Die auffälligsten Beobachtungen: Cannabisextrakte wirken effektiver als isolierte Cannabinoide, und nicht jede Cannabissorte oder Chemovar wirkt gleich. Diese beiden Beobachtungen sind auf ein Phänomen zurückzuführen, das als “Entourage-Effekt” bekannt ist und entsteht, wenn Cannabinoide und andere Cannabis-Verbindungen, wie Terpenoide und Flavonoide, in der Kombination miteinander eingenommen werden und eine veränderte Wirkung entfalten.3 Die zugrunde liegenden Mechanismen sind noch nicht vollständig verstanden und die wichtigsten bioaktiven Verbindungen in Cannabis müssen noch genauer charakterisiert werden, aber auch aufgrund unterschiedlicher Genetik und Wachstumsbedingungen gibt es eine Vielfalt an Möglichkeiten, die zu einer Vielzahl von verschiedenen Ergebnissen führen. Dies zeigte sich auch in einer Studie mit 12 verschiedenen Cannabisextrakten, in welcher deren Fähigkeit in Krebszelllinien den Zelltod zu induzieren, untersucht wurde (Abbildung 2).
Basierend auf den drei Versuchsreihen können einige Aussagen getroffen werden: Nicht jeder Gewebetyp ist von Cannabis betroffen, nicht jedes Cannabisextrakt ist wirksam und für verschiedene Krebstypen sind verschiedene Cannabisextrakte effektiver.
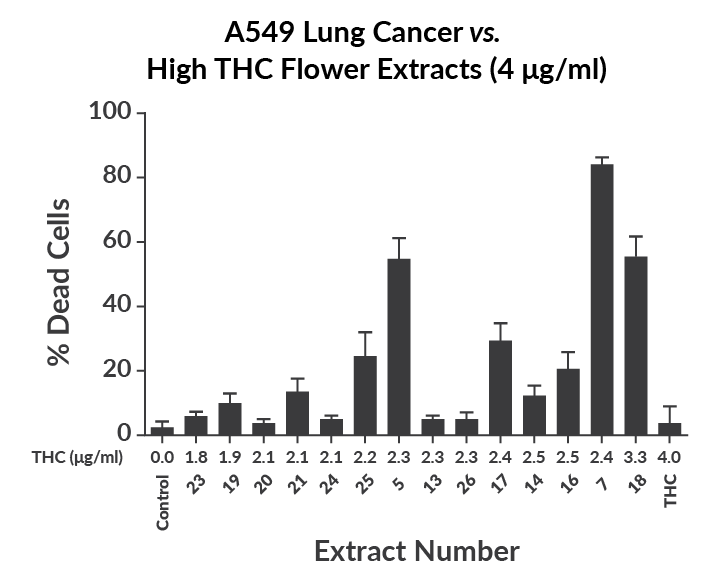
Dies konnte in einer vergleichbaren Untersuchung, die sich auf eine der wichtigsten bioaktiven Verbindungen in Cannabis, Δ9-THC, konzentrierte, bestätigt werden. In dieser in vitro Studie mit 14 Extrakten, die mindestens 18 % Δ9-THC enthielten, und reinem Δ9-THC wurde festgestellt, dass die Cannabisextrakte den Zelltod in A549-Lungenkrebszellen besser induzieren (Abbildung 3). Nach 24 Stunden reichten 4 μg/ml Extrakt aus, um den Zelltod mit mehreren Extrakten zu induzieren. Von den 14 getesteten Extrakten waren drei in der Lage, mehr als die Hälfte der Krebszellen zu töten, wobei einer sogar 80 % abtötete. Dies steht in direktem Gegensatz zu reinem Δ9-THC. Zusätzlich konnte kein Zusammenhang zwischen erhöhter Δ9-THC-Konzentration und erhöhter Effektivität gefunden werden, was auf die Aktivität von zusätzlichen bioaktiven Verbindungen hindeutet.
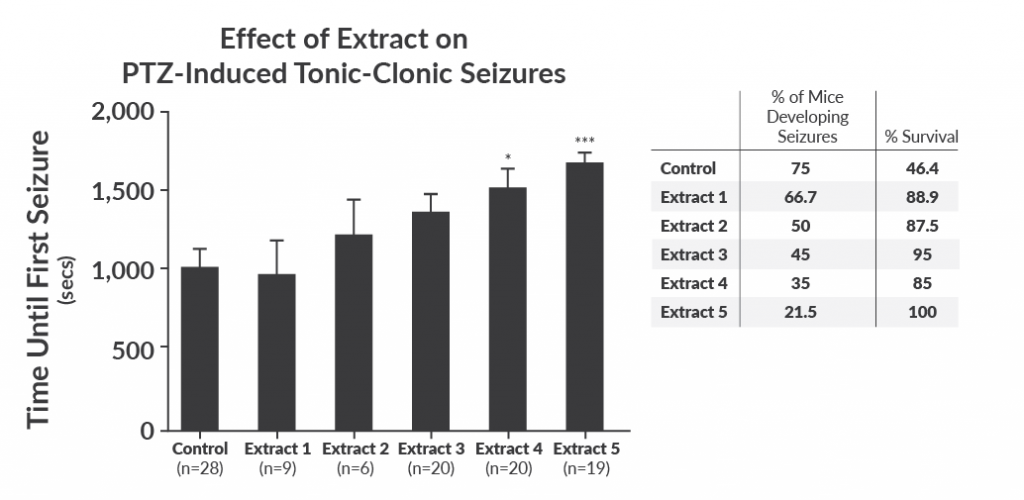
Die gleichen Trends lassen sich bei Pflanzen mit hohem CBD-Gehalt erkennen. In einer in vivo Studie wurden fünf Pflanzen mit hohem CBD-Gehalt und vergleichbaren Konzentration an CBD und Δ9-THC (50% und 2%) auf ihre Wirksamkeit zur Behandlung von Epilepsiesymptomen untersucht (Abbildung 4). Obwohl alle fünf Extrakte ungefähr den gleichen Gehalt an den wichtigsten bioaktiven Substanzen, Δ9-THC und CBD, aufwiesen, waren die Ergebnisse unterschiedlich. Trotzdem verlangen die meisten Behörden auf der ganzen Welt nur, dass die Δ9-THC- und CBD-Werte getestet werden, während biologische Studien zeigen, dass in Wirklichkeit viel mehr Wirkstoffe beteiligt sind.
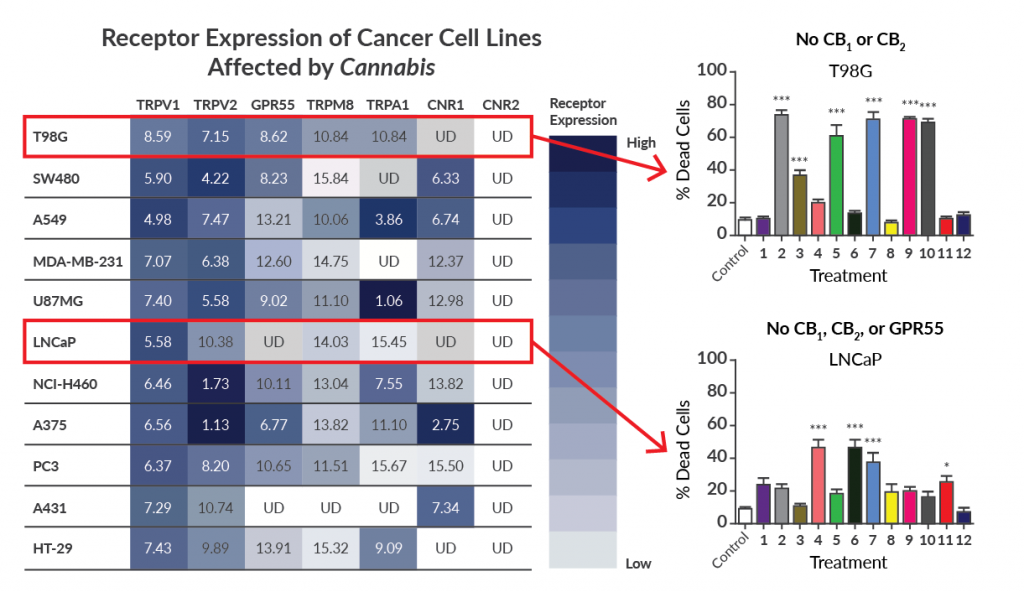
Das therapeutische Potenzial von Cannabis und seinen Bestandteilen wird nie vollständig ausgeschöpft werden können, solange nicht sämtliche bioaktive Verbindungen identifiziert oder eingehendere Tests zum Standard werden. Darüber hinaus ist unser Verständnis des ECSs unvollständig. Wenn wir die Ergebnisse strikt auf der Basis von Interaktionen mit CB1 und CB2 betrachten, ignorieren wir die eigentlichen Grundlagen der Mechanismen. Von den von Baram et al. untersuchten Krebszelllinien zeigten zwei, die stark auf Cannabis reagierten, keine nachweisbare Expression von CB1 oder CB2(Abbildung 5).5 In LNCaP zum Beispiel wurden weder CB1, CB2 noch GPR55 exprimiert (Figure 5).
Die effektive Anwendung von Cannabis hat noch einen langen Weg vor sich, aber Cannabis enthält Verbindungen, die vielversprechende therapeutische Mittel für eine Vielzahl von Erkrankungen sein können. Mit einem breiteren Blick auf das ECS, der über CB1 und CB2 hinausgeht, und dem Verständnis, dass viele Eigenschaften auf mehr als Δ9-THC und CBD zurückzuführen sind, werden wir in der Lage sein, Cannabinoid-basierte Therapien zu verbessern und anzuwenden.
Referenzen
- Di Marzo, V. and Piscitelli, F. The endocannabinoid system and its modulation by phytocannabinoids. Neurotherapeutics 12(4), 692-698 (2015).
- McPartland, J.M. Phylogenomic and chemotaxonomic analysis of the endocannabinoid system. Brain Res. Rev. 45(1), 18-29 (2004).
- Russo, E.B. Taming THC: Potential cannabis synergy and phytocannabinoid‐terpenoid entourage effects. Br. J. Pharmacol. 163(7), 1344-1364 (2011).
- Mechoulam, R. (Ed.) Cannabinoids as therapeutic agents. CRC Press (2019).
- Baram, L., Peled, E., Berman, P., et al. The heterogeneity and complexity of Cannabis extracts as antitumor agents. Oncotarget 10(41), 4091-4106 (2019).
- Berman, P., Futoran, K., Lewitus, G.M., et al. A new ESI-LC/MS approach for comprehensive metabolic profiling of phytocannabinoids in Cannabis. Sci. Rep. 8(1), 14280 (2018).
Author
Ben Euhus, M.Sc.
Source
Biomol, Pressemitteilung, 2021-01-11.
Supplier
Share
Renewable Carbon News – Daily Newsletter
Subscribe to our daily email newsletter – the world's leading newsletter on renewable materials and chemicals














