Bremer Forscher und Forscherinnen am Max-Planck-Institut für marine Mikrobiologie haben ein Bakterium entdeckt, dass als Symbiont die Abfallprodukte seines Wirts in Biomasse umwandelt: Kentron lebt als Untermieter in Wimpertierchen und ist der erste bekannte Schwefel-oxidierende Symbiont, der völlig heterotroph ist.
Pflanzen nutzen die Lichtenergie der Sonne, um mittels Fotosynthese Kohlendioxid (CO2) in Biomasse umzuwandeln. Tiere sind dazu nicht in der Lage. Deshalb haben sich einige von ihnen mit Bakterien zusammengetan, die die sogenannte Chemosynthese beherrschen. Die funktioniert fast wie Fotosynthese, nur dass chemische Energie anstelle von Lichtenergie genutzt wird. Viele Tiere brauchen chemosynthetische Bakterien, die sie mit Nahrung versorgen. Diese Symbionten wandeln CO2 in Biomasse um und werden anschließend von ihrem Wirt verdaut. Kentron, ein Bakterium, das das Wimpertierchen Kentrophoros ernährt, galt bislang als lediglich ein weiterer chemosynthetischer Symbiont. Neue Ergebnisse deuten jedoch darauf hin, dass die Dinge anders liegen.

Aus Abfall wird Nahrung
Ein internationales Team unter der Leitung des Max-Planck-Instituts für marine Mikrobiologie hat das Erbgut von Kentron analysiert, dem Schwefel-oxidierenden Symbionten der Wimpertierchen (Ciliaten). „Entgegen unseren Erwartungen haben wir keines der bekannten Gene entdeckt, die für die Fixierung von CO2 erforderlich sind“, berichtet Erstautor Brandon Seah.
Wenn Kentron kein CO2 binden kann, wovon lebt er dann? „Aus seinen Genen zu schließen, verwendet Kentron kleine organische Verbindungen und verwandelt diese in Biomasse“, erklärt Nicole Dubilier, Direktorin am Max-Planck-Institut für marine Mikrobiologie und leitende Autorin der Studie. Dazu gehören Verbindungen wie Acetat oder Propionat – typische „minderwertige“ Abfallprodukte der Zellen. „So gesehen betreibt Kentron ein Upcycling, es wertet den Abfall auf. Kentron wandelt höchstwahrscheinlich Abfallprodukte aus der Umwelt und von ihren Wirten in höherwertige Biomasse um, um seinen Wirt zu ernähren.“
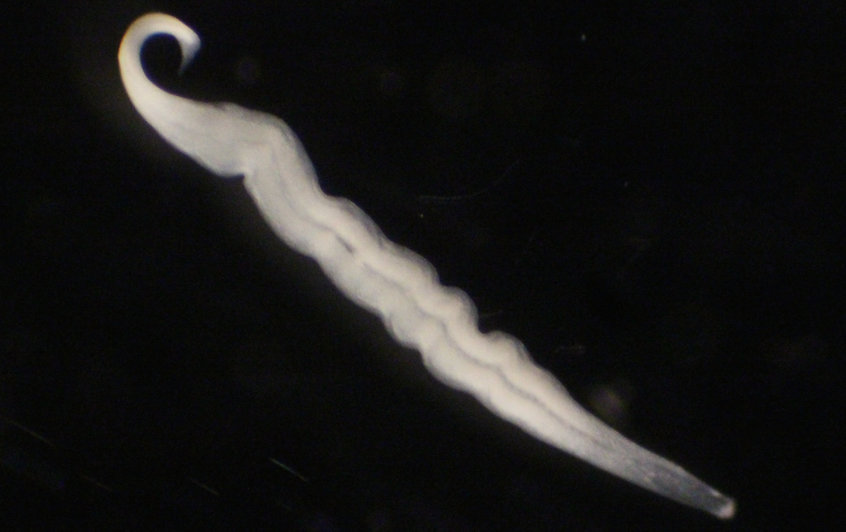
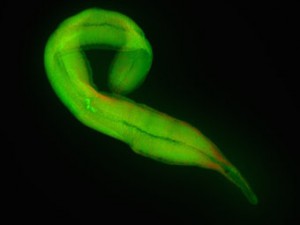
Kentrophoros ist ein dünnes, längliches Wimpertierchen, das in sandigen Meeresböden zuhause ist. Dort kann es leicht zwischen den Sandkörnchen hindurchgleiten. Bei der Ernährung ist es fast vollständig von seinen Symbionten abhängig, es hat nicht einmal mehr einen eigenen Mund. Seah, der mittlerweile am Max-Planck-Institut für Entwicklungsbiologie in Tübingen arbeitet, und seine Kollegen und Kolleginnen sammelten Proben an Standorten im Mittelmeer, der Karibik und der Ostsee. Kentrophoros wächst und vermehrt sich aber nicht im Labor.
Genetische Analysen bestätigt
Wie also konnten die Forscher und Forscherinnen die Ernährungsgewohnheiten von Kentron untersuchen? „Unsere Kollegen in Calgary und North Carolina haben eine Methode entwickelt, um sogar in unseren winzigen Proben den sogenannten Stabile-Isotopen-Fingerabdruck von Proteinen zu messen“, erklärt Seah. Dieser Fingerabdruck verrät einiges darüber, woher ein Organismus seinen Kohlenstoff bezieht. Der Fingerabdruck der Kentron-Bakterien ist ganz anders als jener von anderen chemosynthetischen Symbionten aus ähnlichen Lebensräumen. „Das zeigt deutlich, dass Kentron seinen Kohlenstoff anders bekommt als andere Symbionten.“
Die vorliegenden Ergebnisse liefern ein Gegenbeispiel zur gängigen Lehrbuchmeinung. Diese besagt, dass symbiotische Bakterien den Großteil ihrer Biomasse aus CO2 oder Methan aufbauen. Im Gegensatz dazu scheint es Kentron nicht möglich zu sein, Biomasse so von Grund auf neu zu erzeugen. „Organische Substrate aus der Umwelt aufzunehmen und Abfälle ihrer Wirte zu recyclen könnte in diesen Symbiosen wichtiger sein, als bisher vermutet“, schließt Mitautor Harald Gruber-Vodicka vom Max-Planck-Institut für marine Mikrobiologie. „Das ist bedeutsam für ökologische Modelle des Kohlenstoffkreislaufs in der Umwelt. Wir sind schon gespannt, demnächst die Details und Vor- und Nachteile der beiden Strategien genauer zu untersuchen.”
Kontakte
Prof. Dr. Nicole Dubilier
Max-Planck-Institut für marine Mikrobiologie, Bremen
Tel.: +49 421 2028-932
E-Mail: ndubilie@mpi-bremen.de
Dr. Fanni Aspetsberger
Max-Planck-Institut für marine Mikrobiologie, Bremen
Tel.: +49 421 2028-947
E-Mail: faspetsb@mpi-bremen.de
Originalveröffentlichung
Brandon K. B. Seah, Chakkiath Paul Anthony, Bruno Huettel, Jan Zarzycki, Lennart Schada von Borzyskowski, Tobias J. Erb, Angela Kouris, Manuel Kleiner, Manuel Liebeke, Nicole Dubilier, Harald R. Gruber-Vodicka
‘Sulfur-oxidizing symbionts without canonical genes for autotrophic CO2 fixation’
mBio. DOI: 10.1128/mBio.01112-19
Source
Max-Planck-Gesellschaft, Pressemitteilung, 2019-06-25.
Supplier
Max-Planck-Gesellschaft
Max-Planck-Institut für Entwicklungsbiologie
Max-Planck-Institut für Marine Mikrobiologie
Share
Renewable Carbon News – Daily Newsletter
Subscribe to our daily email newsletter – the world's leading newsletter on renewable materials and chemicals










